Glasmantelsystem zur Untersuchung der Gasgesetze
| Glasmantelsystem zur Untersuchung der Gasgesetze | |
| Versuchsaufbau des Glasmantelsystems | |
| Kurzbeschreibung | |
|---|---|
| Mit dem Glasmantelsystem können experimentell die Zusammenhänge zwischen Druck, Volumen und Temperatur untersucht werden und somit die ideale Gasgleichung hergeleitet werden. | |
| Kategorien | |
| Thermodynamik | |
| Einordnung in den Lehrplan | |
| Geeignet für: | Sek. II |
| Basiskonzept: | Materie, System |
| Sonstiges | |
| Durchführungsform | Demoexperiment |
| Anzahl Experimente in dieser Unterkategorie | 3 |
| Anspruch des Aufbaus | mittel bis schwer |
| Informationen | |
| Name: | Jan Kreienbaum |
| Kontakt: | Fehler beim Parsen (Konvertierungsfehler. Der Server („https://wikimedia.org/api/rest_“) hat berichtet: „Cannot get mml. Server problem.“): {\displaystyle {\text{jan.kreienbaum}}} @ |
| Uni: | Humboldt-Universität zu Berlin |
| Betreuer*in: | Franz Boczianowski |
Mit dem Glasmantelsystem können mit einem Aufbau die Gesetze von Gay-Lussac, Boyle-Mariotte und Amontons experimentell überprüft werden. Diese Gasgesetzte beschreiben die Zusammenhänge zwischen den Zustandsgrößen Volumen, Druck und Temperatur eines idealen Gases. Mit diesen Gasgesetzten lässt sich anschließend die ideale Gasgleichung herleiten. Die Experimente eignen sich daher als ein Einstieg in die Thermodynamik.
Inhaltsverzeichnis
Didaktischer Teil
Aus ihrer alltäglichen Lebenserfahrung haben Schülerinnen und Schüler, teils unbewusst, bereits die Erfahrung gesammelt, dass Luft sich beim Erhitzen ausdehnt, oder bei einer Verringerung des Volumens eines Behälters, in dem sich Luft befindet, der Druck steigt. Allerdings wird nur wenigen die genauen Zusammenhänge zwischen den einzelnen Größen klar sein.
Das Glasmantelsystem bietet die Möglichkeit die Zusammenhänge zwischen den Größen Volumen, Druck und Temperatur eines Gases quantitativ zu untersuchen und die exakten Zusammenhänge experimentell herauszufinden. Die Experimente sollten aufgrund des empfindlichen Aufbaus als Demonstrationsversuch durchgeführt werden. Die Schülerinnen und Schüler können aber sehr gut in die Durchführung mit eingebunden werden, indem sie bei der Aufnahme der Messwerte assistieren.
Folglich liegt der didaktische Schwerpunkt der Experimente im Auswerten und Interpretieren von Daten, sowie im Umgang mit systematischen Messfehlern.
Es ist für physikalisch sauberes Arbeiten wichtig, dass nicht nur Messdaten erhoben werden, sondern aus diesen auch neue Informationen erschlossen werden. Dazu dienen Mittel, wie der Darstellung von gemessenen oder abgeleiteten Größen in Graphen und das anschließende Annähern von Funktionen, um Zusammenhänge zwischen den dargestellten Größen zu untersuchen. Diese Fitfunktionen gilt es wiederum zu interpretieren und für Unstimmigkeiten mit der zugrundeliegenden Theorie Erklärungen zu finden. Abschließend gilt es aus den in der Auswertung produzierten Daten auf Gesetzmäßigkeiten zu schließen.
Diese, oder zu mindestens einige dieser, Schritte können die Schülerinnen und Schüler in der Auswertung der Versuche mit dem Gasthermometer zu den Gasgesetzten nachvollziehen. Bei der Auswertung der hier vorgestellten Versuche müssen besonders systematische Messfehler beachtet werden (siehe unten). Wahrscheinlich müssen die Schülerinnen und Schüler dazu angeleitet werden, besonders im Umgang mit den Fitfunktionen und deren Offsets die Werte kritisch zu hinterfragen und dazu ermutigt werden, die Ursachen für unstimmige Ergebnisse am Aufbau selbst zu suchen.
Für die Gestaltung des Unterrichts ist es ratsam die Schülerinnen und Schüler in Kleingruppen arbeiten zu lassen. Es wäre darüber hinaus von Vorteil, wenn für die Auswertung und Erstellung der Graphen Computer mit entsprechenden Programmen zur Verfügung stehen würden. Die Auswertung sollte (zum Beispiel durch ein Arbeitsblatt) angeleitet erfolgen, die Lehrkraft hat dabei eine passive, beratende Rolle inne.
Gelingt es den Schülerinnen und Schülern aus den Messwerten Gesetzmäßigkeiten abzuleiten, so ist dies zum einem ein Erfolgserlebnis, zum anderen werden sie aber wesentlich sicherer im Umgang mit Daten und lernen, die Versuchsanordnung kritisch auf mögliche Probleme zu untersuchen.
Versuchsanleitung
Die Versuche wurden mit Hilfe des Handbuchs zum Glasmantelsystem von Phywe[1] durchgeführt.
Aufbau
Materialien
- Glasmantel (Phywe, 02615.00)
- Gasspritze 100 ml (Phywe, 02614.00)
- 2 Laborthermometer (-10...+150°C)
- Digitales Manometer (hier: CorEx EasySense VISION, Cornelsen Experiments 740055)
- Heizplatte 32246.93
- H-Fuß
- 2 Stativstangen lang (min. 70 cm)
- 1 Stativstange kurz (ca. 20 cm)
- 2 Tischklemmen
- 5 Doppelmuffen
- 3 Universalklemmen
- 2 Silikonschläuche (ø 7 mm)
- 1 Verbindungsstück für Schläuche
- 1 Magnetstäbchen in Schrumpfgummi (ca. 5 cm)
- 1 Stabmagnet
- Becherglas
- 2 Gummi Stopfen mit Loch (ø 7 mm)
- Motorenöl
- Pipette
- Draht
- Trichter
Einbauen der Gasspritze in den Glasmantel
Zunächst muss die Überwurfmutter an der breiten Öffnung des Glasmantels gelöst und die Schraubverbindungskappe an der kleineren Öffnung gelockert werden.
Die Gasspritze wird durch die Überwurfmutter und den Dichtungsring in den Glasmantel eingeführt. Die Spritze wird so weit hineingeschoben, bis die Spitze auf der anderen Seite durch den Stutzen wieder herausschaut.
Nun wird zunächst die Schraubverbindungskappe festgezogen und anschließend die Überwurfmutter mit dem Schraubring verschraubt. Dabei ist darauf zu achten, dass die Dichtung die Öffnung des Glasmantels komplett abdeckt.
Eigentlicher Versuchsaufbau
Das Glasmantelsystem wird mit den Universalklemmen an die beiden langen Stativstangen befestigt. Dabei greift die eine Universalklemme um die Überwurfmutter und die zweite um die Schraubverbindungskappe des Glasmantels. Der Glasmantel ist in einer solchen Höhe anzubringen, dass die Heißplatte auf dem H-Fuß problemfrei darunter geschoben werden kann.
Auf die Kanüle der Spritze wird ein kurzer Silikonschlauch gezogen und eventuell mit einem kurzen Draht befestigt. Das andere Ende des Schlauches bleibt bis zum Ende des Aufbauens offen, da die Spritze sonst nicht mehr zu bewegen wäre.
Der Glasmantel wird durch eine der oberen Öffnungen mit Wasser gefüllt, bis dass die Spritze im Inneren komplett vom Wasser umgeben ist. Das Magnetstäbchen wird mit hineingeworfen und anschließen wird in beide der oberen Öffnungen ein Stopfen mit Loch gesetzt und je ein Thermometer durch diese bis ins Wasser eingeführt. Da die Gasspritze vollkommen vom Wasser umgeben ist, kann davon ausgegangen werden, dass die Temperatur der Luft in der Spritze der des Wassers entspricht.
An die verbleibende obere Öffnung wird ein Silikonschlauch angeschlossen, welcher in einem mit Wasser gefülltes Becherglas endet. Es bietet sich an, das Becherglas mit einer Universalklemme zu fixieren. Dieser Schlauch dient dazu heiße Luft und entstehenden Wasserdampf aus dem Inneren des Glasmantels abzuleiten.
Die kurze Stativstange wird mit einer Doppelmuffe an die rechte Stativstange befestigt und parallel zum Kolben der Spritze ausgerichtet.
Um Entweichen der Luft aus der Spritze zu vermeiden, wird etwas Motorenöl mit einer Pipette auf den Spritzenkolben gegeben, bevor dieser soweit in die Spritze gesteckt wird, dass er ein Luftvolumen von 50 ml einschließt. Dabei ist darauf zu achten, dass sich zwischen Kolben und Spritzenwand ein gleichmäßiger Ölfilm bildet. Es ist ratsam unter dem Ende der Spritze ein Tuch auszulegen, da Motorenöl herauslaufen und heruntertropfen kann.
Zum Schluss wird der Schlauch, der an der Kanüle der Spritze befestigt ist, mit einem Verbindungsstück an den Drucksensor angeschlossen.
Vor der Messung ist es ausgesprochen wichtig, die Dichtheit des Aufbaus zu überprüfen. Dazu wird das digitale Manometer eingeschaltet und der Druck notiert. Anschließend wird der Kolben hereingeschoben, so dass das Luftvolumen auf 35 ml komprimiert wird. Nach kurzem Warten, wird der Kolben wieder soweit herausgezogen, bis er wieder bei 50 ml steht. Der nun gemessene Druck sollte mit dem zuvor notierten übereinstimmen. Weicht er ab, müssen alle Verbindungsstellen des Schlauches und die Ölung des Kolben erneut überprüft werden und gegebenenfalls mit Draht fixiert oder nachgeölt werden.
Versuch 1: Gesetz von Gay-Lussac
Das Gesetz von Gay-Lussac beschreibt den Zusammenhang zwischen dem Volumen Fehler beim Parsen (Konvertierungsfehler. Der Server („https://wikimedia.org/api/rest_“) hat berichtet: „Cannot get mml. Server problem.“): {\displaystyle V} und der Temperatur eines idealen Gases bei konstantem Druck .
Durchführung
Das digitale Monometer und beide Thermometer werden eingeschaltet und die jeweiligen Werte bei einem Volumen von 50 ml notiert. Die Heißplatte auf dem H-Fuß wird unter das Glasmantelsystem geschoben und an den Zylinder angenähert, bis ein leichter Kontakt besteht. Die Heißplatte wird eingeschaltet und mit dem Stabmagneten wird das Magnetstäbchen im Inneren des Glasmantels so bewegt, dass das Wasser in Bewegung bleibt und somit gleichmäßig erwärmt wird. Wenn die Werte auf beiden Thermometern zu stark voneinander abweichen, muss stärker gerührt werden.
Durch die Erwärmung der Luft in der Spritze dehnt diese sich aus und drückt den Kolben heraus. Eventuell muss der Kolben leicht angestoßen werden oder von Hand herausgezogen werden. Dabei ist immer dafür zu sorgen, dass der Druck konstant bleibt.
Bei jedr 15°C Temperaturerhöhung wird das Luftvolumen an der Gasspritze abgelesen und notiert. Die Messreihe kann bis 100°C geführt werden. Für die Auswertung wird die Temperatur in Kelvin umgerechnet. Wichtig ist es zu beachten, dass nach dem Erreichen von 100°C die Heizplatte ausgeschaltet und entfernt wird, um zu vermeiden, dass der Druck im Inneren des Glasmantels zu hoch wird.
Ergebnisse
Die Ergebnisse der Messung sind in der folgenden Tabelle dargestellt:
| Temperatur [K] | Volumen [ml] | |
|---|---|---|
| Fehler beim Parsen (Konvertierungsfehler. Der Server („https://wikimedia.org/api/rest_“) hat berichtet: „Cannot get mml. Server problem.“): {\displaystyle 296,05\pm 0,5} | Fehler beim Parsen (Konvertierungsfehler. Der Server („https://wikimedia.org/api/rest_“) hat berichtet: „Cannot get mml. Server problem.“): {\displaystyle 0,17\pm 0,01} | |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 303,85 \pm 0,5 } | Fehler beim Parsen (Konvertierungsfehler. Der Server („https://wikimedia.org/api/rest_“) hat berichtet: „Cannot get mml. Server problem.“): {\displaystyle 51,1\pm 0,5} | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,17 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 318,45 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 54,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,17 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 335,25 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 57,5 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,17 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 347,75 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 60 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,17 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 364,65 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 63 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,17 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 372,15 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 64,5 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,17 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 373,15 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 65 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,17 \pm 0,01 } |
Auswertung
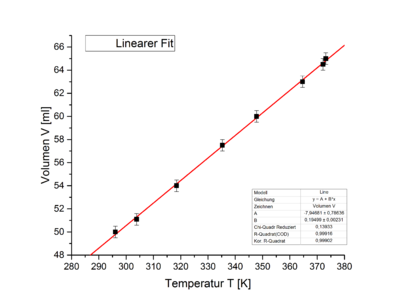
In Abbildung 5 sind die Messwerte in einem V-T-Diagramm dargestellt. Der proportionale Zusammenhang zwischen Temperatur und Druck ist leicht zu erkennen und wird durch den linearen Fit (rot) verdeutlicht. Beim Fit ergibt sich ein Offset von Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle V_0=(7,9\pm0,8)}
ml. Dieser Offset entspricht dem Volumen des Schlauches zwischen der Gasspritze und dem Drucksensor und kann zur Korrektur der weiteren Messungen verwendet werden.
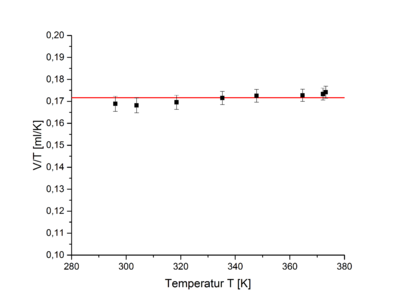
Wird statt dem Volumen der Quotient aus V und T gegen T aufgetragen ergibt sich der Graph in Abb. 6. Dort ist gut zu erkennen, dass dieser Quotient konstant ist. Also folgt Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle V \propto T}
.
Daher gilt bei dem Übergang eines Systems vom Zustand 1 mit Volumen Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle V_1}
und Temperatur Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle T_1}
in den Zustand 2 mit Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle V_2}
und Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle T_2}
mit konstantem Druck:
Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \frac{V_1}{T_1}=\frac{V_2}{T_2}}
Versuch 2: Gesetz von Boyle-Mariotte
Das Gesetz von Boyle-Mariotte beschreibt den Zusammenhang zwischen dem Volumen Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle V } und dem Druck Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle p } eines idealen Gases bei konstanter Temperatur Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle T } .
Durchführung
Das digitale Manometer wird eingeschaltet und der Druck bei einem Volumen von 50 ml notiert. Anschließend wird der Kolben stückweise herausgezogen, so dass das Volumen in 2 ml Schritten bis auf 60 ml expandiert wird. Zu jedem Volumen wird der Druck gemessen und notiert. Anschließend wird der Kolben wieder bis zum Ausgangspunkt hereingeschoben und das Volumen nun in 2 ml Schritten auf 40 ml komprimiert. Erneut wird der Druck gemessen. Für die Auswertung kann es interessant sein, auch ein oder zwei weitere Messwerte für den Druck bei einem Volumen unter 40 ml oder über 60 ml zu nehmen.
Ergebnisse
Bei der Messung des Drucks ergaben sich folgende Werte:
| Volumen [ml] | Druck [kPa] | Druck Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \cdot} Volumen [Nm] |
|---|---|---|
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 35,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 132,3 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 4,63 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 40,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 119,1 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 4,76 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 42,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 114,8 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 4,82 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 44,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 110,7 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 4,87 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 46,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 106,7 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 4,90 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 48,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 103,1 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 4,94 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 50,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 99,2 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 4,96 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 52,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 96,2 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,00 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 54,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 93,2 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,03 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 56,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 90,4 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,06 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 58,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 87,5 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,07 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 60,0 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 85,3 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,12 \pm 0,07 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 65,0 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 78,9 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,13 \pm 0,10 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 70,0 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 74,6 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,22 \pm 0,10 } |
Auswertung
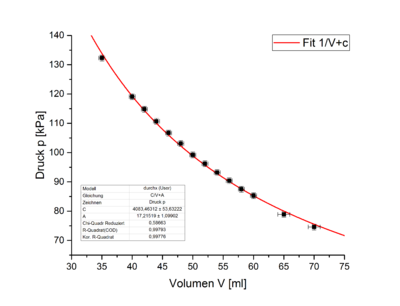
Werden die Daten in ein p-V-Diagramm übertragen, so ist ein Antiproportionaler Zusammenhang zwischen dem Volumen und dem Druck zu erkennen.
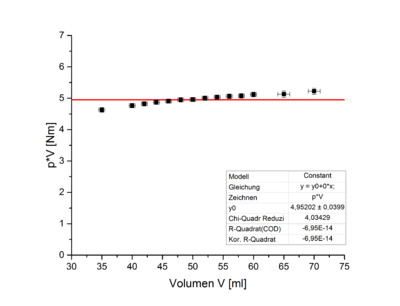
Wird das Produkt aus Druck und Volumen gegen das Volumen aufgetragen, so ist zu erwarten, dass dieses Verhältnis konstant ist. Wie in Abbildung 8 jedoch zu sehen ist, trifft dies nicht zu. Die Abweichung der Messpunkte von der waagerechten Linie sind deutlich größer als der Messfehler.
Diese Abweichung ist durch das Volumen des Schlauches zu erklären, welches oben bereits zu Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle (7,9\pm0,8)}
ml ermittelt wurde. Werden die Messwerte für das Volumen um dieses "Totvolumen" korrigiert, so ergeben sich folgende Messwerte:
| Volumen [ml] | Druck [kPa] | Druck Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \cdot} Volumen [Nm] |
|---|---|---|
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 42,9 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 132,3 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,68 \pm 0,18 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 47,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 119,1 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,70 \pm 0,16 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 49,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 114,8 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,72 \pm 0,16 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 51,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 110,7 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,74 \pm 0,15 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 53,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 106,7 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,75 \pm 0,15 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 55,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 103,1 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,77 \pm 0,15} |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 57,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 99,2 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,74 \pm 0,14 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 59,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 96,2 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,76 \pm 0,14 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 61,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 93,2 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,80 \pm 0,14 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 63,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 90,4 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,78 \pm 0,13 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 65,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 87,5 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,77 \pm 0,13 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 67,9 \pm 1,3 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 85,3 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,80 \pm 0,13 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 72,9 \pm 1,8 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 78,9 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,75 \pm 0,16 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 77,9 \pm 1,8 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 74,6 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 5,81 \pm 0,16 } |
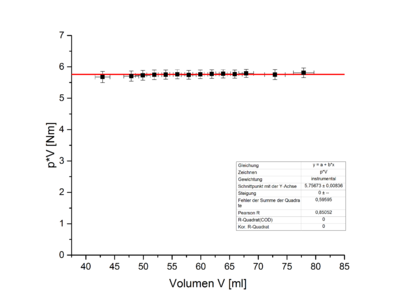
Wird nun mit den neuen Werten das Produkt aus Druck und Volumen gegen das Volumen abgetragen (sieh Abb. 9) ist das konstante Verhalten des Produkts aus Druck und Volumen sehr gut zu erkennen.
Daraus folgt, dass Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle p \propto \frac{1}{V}}
.
Daher gilt bei dem Übergang eines Systems vom Zustand 1 mit Volumen Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle V_1}
und DruckFehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle p_1}
in den Zustand 2 mit Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle V_2}
und Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle p_2}
mit konstanter Temperatur:
Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle V_1 \cdot p_1 = V_2 \cdot p_2 }
Versuch 3: Gesetz von Amontons
Das Gesetz von Amontons beschreibt den Zusammenhang zwischen der Temperatur Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle T } und dem Druck Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle p } eines idealen Gases bei konstantem Volumen Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle V } .
Durchführung
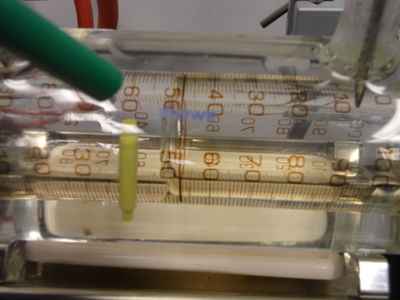
Der Kolben der Gasspritze wird mit einer Universalklemme, welche an der kurzen Stativstange befestigt wird, auf ein Volumen von 50 ml fixiert (siehe Abb. 10). Dabei ist darauf zu achten, dass sich der Kolben wirklich nicht mehr verschieben lässt.
Das digitale Monometer und beide Thermometer werden eingeschaltet und die jeweiligen Werte notiert. Der H-Fuß mit der Heißplatte wird unter das Glasmantelsystem geschoben und heraufgefahren, bis ein leichter Kontakt besteht. Die Heizplatte wird eingeschaltet und mit dem Stabmagneten und dem Magnetstäbchen das Wasser so umgerührt, dass sich die Temperaturen auf beiden Thermometern nie zu stark unterscheide.
Bei jeder 15°C Temperaturerhöhung wird der Druck auf dem digitalen Manometer abgelesen, bis eine Temperatur von 100°C erreicht ist. Auch hier wurden die Messwerte anschließend in Kelvin umgerechnet. Während des Erhitzens ist es wichtig, regelmäßig die Position des Glaskolbens zu beobachten, und sicher zu gehen, dass das Volumen konstant bleibt. Nach Erreichen der maximalen Temperatur muss die Heizplatte ausgeschaltet und entfernt werden.
Ergebnisse
Bei der Messung ergaben sich folgende Werte:
| Temperatur [K] | Druck [kPa] | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \frac{\text{Druck}}{\text{Temperatur}}\left[\frac{\text{kPa}}{\text{K}}\right]} |
|---|---|---|
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 296,05 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 99,8 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,34 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 303,85 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 102,0 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,34 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 318,45 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 107,5 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,34 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 335,25 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 112,0 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,33 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 347,75 \pm 0,5 } | Fehler beim Parsen (Konvertierungsfehler. Der Server („https://wikimedia.org/api/rest_“) hat berichtet: „Cannot get mml. Server problem.“): {\displaystyle 115,5\pm 1,0} | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,33 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 364,65 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 120,4 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,33 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 372,15 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 122,5 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,33 \pm 0,01 } |
| Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 373,15 \pm 0,5 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 123,1 \pm 1,0 } | Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle 0,33 \pm 0,01 } |
Auswertung
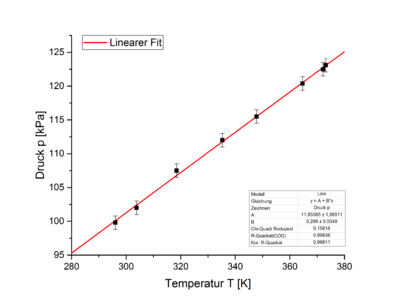
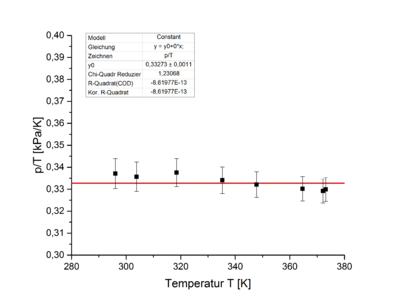
In Abbildung 11 sind die Messwerte in einem p-T-Diagramm dargestellt. Der lineare Fit (rote Linie) verdeutlicht, dass ein linearer Zusammenhang besteht. Der Fit hat einen Offset von Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle p_0=(11,9\pm1,6)kPa}
. Es wurde jedoch, wie bei den Messung zuvor, ein proportionaler Zusammenhang erwartet. Der Offset wird vermutlich dadurch verursacht, dass der Aufbau nicht komplett abgedichtet war und auch dadurch, dass sich das Schlauchstück bei hohem Druck ausdehnt, beziehungsweise bei niedrigem Druck zusammenzieht.
Das dieser Fehler jedoch vernachlässigbar ist, zeigt sich wenn der Quotient von Druck und Temperatur gegen die Temperatur abgetragen wird (siehe Abb.12).
Dieser Graph zeigt, dass sich der Druck proportional zur Temperatur verhält: Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle p \propto T}
.
Folglich gilt bei dem Übergang eines Systems vom Zustand 1 mit Temperatur Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle T_1}
und Druck Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle p_1}
in den Zustand 2 mit Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle T_2}
und Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle p_2}
mit konstantem Druck:
Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \frac{p_1}{T_1}\frac{p_2}{T_2}}
Zusammenfassung und Anmerkungen
Das Glasmantelsystem eignet sich sehr gut dazu die Gasgesetzte empirisch zu untersuchen und Daten zu den einzelnen Gesetzten aufzunehmen. In einer einzigen Stunde können problemlos Messdaten zu zwei der drei Gasgesetzte aufgenommen werden, ohne den Versuchsaufbau zu verändern. So kann zum Beispiel zuerst das Gesetzt von Boyle-Mariotte untersucht werden und im Anschluss die Heizplatte eingeschaltet und das Gesetzt von Gay-Lussac betrachtet werden. Da das Erhitzen bis auf 100°C bis zu 15 Minuten dauern kann, ist es zu empfehlen nur zwei oder drei Werte zum Gesetz von Gay-Lussac aufzunehmen und den Schülerinnen und Schülern anschließend eine zuvor angefertigte Datenreihe zu geben.
Die Kombination dieser beiden Versuche bietet sich an, da die in dem einem Versuch auftretenden Messfehler durch die Ergebnisse des anderen Versuchs erklärt und korrigiert werden können. Darüber hinaus genügen diese beiden Gesetzte, um die Gasgleichung für ideale Gase herzuleiten[2].
Die Versuchsanleitung im Handbuch von Phywe[1] schlägt vor, die Gesetzte von Gay-Lussac und Amontons gleichzeitig zu untersuchen, indem bei jeden 15°C Schritt zunächst das veränderte Volumen notiert wird und anschließend der Kolben wieder auf die Ausgangsposition hereingeschoben wird und dann der Druck gemessen wird. Gewiss ist es so möglich, alle drei Gasgesetze in einem einzigen Messdurchgang zu untersuchen, jedoch besteht die Gefahr, dass es für die Schülerinnen und Schüler nicht ersichtlich wird, dass bei gleichbleibenden Volumen und steigender Temperatur der Druck steigt. Vielmehr sehen sie, dass bei steigender Temperatur das Volumen zunimmt und anschließend, bei einer Kompression der Luft der Druck steigt. Auch aus diesem Grund ist es empfohlen, nur zwei der drei Gesetzte in einem Durchgang zu messen.
Es ist zu beachten, dass der Aufbau recht anfällig für Messfehler ist. Besonders das Abdichten der Spritze und Verbindungsschläuche stellt immer wieder ein Problem dar.
Sicherheitshinweise
- Die Heizplatte und auch der Glasmantel werden sehr heiß!
- Beim Erhitzen des Wassers entsteht im Inneren des Glasmantels Wasserdampf und dadurch großer Druck. Es ist immer darauf zu achten, dass die Luft aus dem Mantel über den Schlauch entweichen kann!
- Wird der Druck in der Gasspritze, durch starkes hereinschieben des Kolbens oder hohe Temperaturen, zu stark erhöht, so kann der Verbindungsschlauch zum Drucksensor abfliegen!
- Mit dem Motorenöl ist immer sparsam umzugehen und es wird dringend empfohlen ein Tuch unterzulegen!
Literatur
- ↑ 1,0 1,1 F. Lindenblatt, W. Jung: Handbuch Glasmantel. Phywe Schriftenreihe, Göttingen, 1993.
- ↑ https://www.uni-ulm.de/fileadmin/website_uni_ulm/nawi.inst.251/Didactics/thermodynamik/INHALT/IDEAL.HTM







![{\displaystyle {\frac {\text{Volumen}}{\text{Temperatur}}}\left[{\frac {\text{ml}}{\text{K}}}\right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d9435090674474a34e488bedcdbe250254227286)